 400-028-6288
400-028-6288 在线客服
在线客服
 官方微信
官方微信
 400-028-6288
400-028-6288 在线客服
在线客服
 官方微信
官方微信

替诺福韦二代(Vemlidy)
全部名称:
富马酸丙酚替诺福韦片、替诺福韦、韦立得、Vemlidy、Tenofovir alafenamide、TAF、替诺福韦二代
适应症:
用于治疗6岁及以上、体重至少25千克的成人和儿童慢性乙型肝炎病毒(HBV)感染伴代偿性肝病。
 海外直邮
海外直邮 药师指导
药师指导 隐私服务
隐私服务 签订合同
签订合同
(以下内容仅供参考,具体用药详情请谨遵医嘱)
用法用量(具体用药详情请谨遵医嘱)
1、替诺福韦(韦立得、Vemlidy、TAF)使用前的测试
在开始替诺福韦(韦立得、Vemlidy、TAF)治疗前,应对患者进行HIV-1感染检测。HIV-1感染患者不应单独使用替诺福韦(韦立得、Vemlidy、TAF)。
在开始替诺福韦(韦立得、Vemlidy、TAF)之前或之时,以及在使用替诺福韦(韦立得、Vemlidy、TAF)进行临床适当治疗期间,评估所有患者的血清肌酸酐、估计肌酐清除率、尿糖和尿蛋白。对于慢性肾病患者,还要评估血清磷。
2、6岁及以上体重至少25千克的成人和儿童患者的推荐剂量
6岁及以上、体重至少25千克的成人和儿童患者服用替诺福韦(韦立得、Vemlidy、TAF)的推荐剂量为每日一次,随食物口服一片25毫克片剂。
3、肾功能损害患者的剂量
对于估计肌酐清除率大于或等于15毫升/分钟的患者,或患有终末期肾病的患者,无需调整替诺福韦(韦立得、Vemlidy、TAF)的剂量(ESRD;估计肌酐清除率低于15毫升/分钟),正在接受慢性血液透析。在血液透析的天数内,在血液透析治疗结束后给药。
对于未接受慢性血液透析的ESRD病患者,不建议使用替诺福韦(韦立得、Vemlidy、TAF)。
尚无数据可用于在肾功能损害的儿童患者中提出剂量建议。
4、肝功能损害患者的剂量
轻度肝功能损害患者(Child-Pugh A)无需调整替诺福韦(韦立得、Vemlidy、TAF)的剂量。对于失代偿性(Child- Pugh B或C)肝功能损害的患者,不建议使用替诺福韦(韦立得、Vemlidy、TAF)。
不良反应
1、乙型肝炎严重急性加重
2、肾功能损害新发或恶化
3、乳酸性酸中毒/严重肝肿大伴脂肪变性
4、常见副作用:头痛
禁忌症
1. 对本药品中任何一种成分过敏者应禁用。
2. 孕妇妊娠期妇女用药前需经专业医生仔细评估后,在利大于弊的情况下才可使用。
3. 哺乳期妇女有研究表明,替诺福韦可以少量分泌到乳汁中,但乳汁中的剂量是否会对哺乳期婴儿产生影响目前尚未明确。因此,正在接受替诺福韦治疗的哺乳期妇女,为安全起见不建议母乳喂养。
4. 儿童使用替诺福韦治疗慢性乙型肝炎对于12岁以下儿童的安全性及有效性尚未确定,不推荐给予12岁以下儿童使用该药治疗慢性乙肝。
5. 肾功能不全者慎用。
6. 老年患者的心功能以及肝、肾功能均会有所下降,且合并其他疾病正在服用其他药物的几率也会增加,发生药物不良反应及药物相互作用的概率相对高一些。故老年人用药应在医生权衡后,利大于弊时谨慎使用,且选择剂量时也应谨慎。服药期间应该密切监测肝、肾功能。
7. 禁止联用阿德福韦酯:替诺福韦与阿德福韦酯合用时,由于两种药可竞争肾小管排泌,使两药的肾清除率均降低,两种药的血药浓度均会升高,出现肾脏毒性的概率也会明显增加。因此,不推荐两种药联用于乙型肝炎患者的抗病毒治疗。
8. 谨慎联用去羟肌酐:替诺福韦与去羟肌酐合用可显著增加去羟肌酐的血浆浓度,较高的去羟肌酐浓度可能引起胰腺炎、外周神经病变、CD4细胞计数减少、腹泻、严重的乳酸性酸中毒等不良反应。去羟肌酐与替诺福韦联用时应适当减量。
9. 其他经肾脏消除的药物:替诺福韦与阿德福韦酯、西多福韦、阿昔洛韦、更昔洛韦等其他经肾脏消除的药物合用时,替诺福韦以及其他经肾脏清除的药物浓度会增高,应密切监测替诺福韦等药物相关的不良反应。
10. 洛匹那韦/利托那韦:替诺福韦与洛匹那韦/利托那韦合用可使替诺福韦的浓度增加,应当密切监测替诺福韦相关的药物不良反应。
11. 阿扎那韦:阿扎那韦与替诺福韦合用时,可使替诺福韦的浓度增加,同时阿扎那韦的浓度会降低。因此,两药合用治疗HIV-1感染时需同时联合利托那韦,并注意监测替诺福韦的药物不良反应。
12. 来迪派韦/索磷布韦:来迪派韦/索磷布韦与替诺福韦联合用药时,可使替诺福韦的浓度增加,应密切监测替诺福韦相关的药物不良反应。
注意事项
1、停止治疗后的乙型肝炎严重急性恶化
停止包括替诺福韦(韦立得、Vemlidy、TAF)在内的抗乙型肝炎治疗可能导致乙型肝炎严重急性加重。应密切监测停止替诺福韦(韦立得、Vemlidy、TAF)治疗的患者,在停止治疗后至少进行几个月的临床和实验室随访。如果合适,可能需要恢复抗乙肝病毒治疗。
2、HBV和HIV-1合并感染患者产生HIV-1耐药性的风险
由于存在产生HIV-1耐药性的风险,因此不建议单独使用替诺福韦(韦立得、Vemlidy、TAF)治疗HIV-1感染。在HBV和HIV-1合并感染的患者中,替诺福韦(韦立得、Vemlidy、TAF)的安全性和疗效尚未确定。在开始替诺福韦(韦立得、Vemlidy、TAF)治疗前,应向所有HBV感染患者提供HIV抗体检测,如果检测结果为阳性,则应使用推荐用于HIV-1合并感染患者的适当抗逆转录病毒联合治疗方案。
3、新发或恶化的肾功能损害
含TAF产品上市后曾有肾功能损害病例报告,包括急性肾衰竭、近端肾小管病变(PRT)和范科尼综合征;虽然这些病例的大多数特征为可能导致所报告的肾脏事件的潜在混杂因素,但也有可能这些因素使患者易发生替诺福韦(韦立得、Vemlidy、TAF)相关的不良事件。
服用替诺福韦(韦立得、Vemlidy、TAF)前体药物的肾功能受损患者和服用肾毒性药物(包括非甾体抗炎药)的患者发生肾脏相关不良反应的风险增加。
在开始使用替诺福韦(韦立得、Vemlidy、TAF)之前或之时,以及在使用替诺福韦(韦立得、Vemlidy、TAF)进行临床适当治疗期间,评估所有患者的血清肌酸酐、估计肌酐清除率、尿糖和尿蛋白。对于慢性肾病患者,还要评估血清磷。对于出现临床意义上的肾功能显著下降或范科尼综合征迹象的患者,停用替诺福韦(韦立得、Vemlidy、TAF)。
4、乳酸性酸中毒/严重肝肿大伴脂肪变性
单独使用核苷类似物[包括富马酸替诺福韦二吡呋酯(TDF),替诺福韦的另一种前药]或与其他抗逆转录病毒药物联合使用时,曾有发生乳酸性酸中毒和严重肝肿大伴脂肪变性的报告,包括出现致死病例。对于出现提示乳酸性酸中毒或明显肝毒性(可能包括肝肿大和脂肪变性,即使转氨酶没有显著升高)的临床或实验室检查结果的患者,应暂停替诺福韦(韦立得、Vemlidy、TAF)治疗。
特殊人群用药
1、妊娠期
在动物研究中,如果在器官形成期使用替诺福韦(韦立得、Vemlidy、TAF),其暴露量为等于或51倍的推荐替诺福韦(韦立得、Vemlidy、TAF)日剂量,未观察到对发育的不良影响。在哺乳期内服用TDF,其替诺福韦暴露量约为替诺福韦(韦立得、Vemlidy、TAF)推荐日剂量暴露量的12倍,未观察到对后代的不良影响。
在动物中进行的胚胎-胎儿发育研究显示,没有证据表明生育力受损或对胎儿造成伤害。
2、哺乳期
已发表文献中的数据报告了母乳中存在替诺福韦(韦立得、Vemlidy、TAF)。已发表文献中的数据未报告替诺福韦(韦立得、Vemlidy、TAF)对母乳喂养儿童的不良影响。没有关于替诺福韦(韦立得、Vemlidy、TAF)对乳汁产量的影响的数据。
在考虑母乳喂养对发育和健康的益处的同时,还应考虑母亲对替诺福韦(韦立得、Vemlidy、TAF)的临床需求以及替诺福韦(韦立得、Vemlidy、TAF)或潜在母体疾病对母乳喂养婴儿的任何潜在不良影响。
3、儿童使用
在试验1092中,已在6岁至18岁且体重至少25千克(N=59)的儿童患者中确定了替诺福韦(韦立得、Vemlidy、TAF)治疗慢性HBV感染的药代动力学、安全性和有效性,时间长达96周。与在成人中观察到的差异相比,在药代动力学或安全性方面未观察到具有临床意义的差异。
在年龄小于6岁或体重小于25公斤的儿童慢性HBV感染患者中,替诺福韦(韦立得、Vemlidy、TAF)的安全性和有效性尚未确定。
4、老年用药
在临床试验中,对89名年龄在65岁及以上的受试者给予替诺福韦(韦立得、Vemlidy、TAF)。未观察到老年受试者与18岁至65岁之间的受试者之间在安全性或疗效方面存在具有临床意义的差异。
5、肾功能损害
对于轻度、中度或重度肾功能损害的患者,或正在接受慢性血液透析的ESRD(估计肌酐清除率低于15毫升/分钟)患者,无需调整替诺福韦(韦立得、Vemlidy、TAF)的剂量。在血液透析当天,在完成血液透析治疗后服用替诺福韦(韦立得、Vemlidy、TAF)。
在接受慢性血液透析和服用替诺福韦(韦立得、Vemlidy、TAF)的ESRD病受试者中,在HBV感染受试者(试验4035部分)中观察到的替诺福韦暴露量高于HIV感染受试者(试验1825)。尚未确定这些较高暴露量的临床意义。
不建议在未接受慢性血液透析的ESRD(通过Cockcroft-Gault法估计肌酐清除率低于15毫升/分钟)患者中使用替诺福韦(韦立得、Vemlidy、TAF),因为尚未在该人群中确定替诺福韦(韦立得、Vemlidy、TAF)的安全性。
6、肝功能损害
轻度肝功能损害患者(Child-Pugh A)无需调整替诺福韦(韦立得、Vemlidy、TAF)的剂量。在失代偿性肝硬化(Child-Pugh B或C)患者中使用替诺福韦(韦立得、Vemlidy、TAF)的安全性和疗效尚未确定;因此,不建议在失代偿性(Child-Pugh B或C)肝功能损害患者中使用替诺福韦(韦立得、Vemlidy、TAF)。
药物相互作用
1、其他药物影响替诺福韦(韦立得、Vemlidy、TAF)的可能性
替诺福韦(韦立得、Vemlidy、TAF)是P-糖蛋白(P-gp)和BCRP的底物。强烈影响P-gp和BCRP活性的药物可能会导致替诺福韦酯的吸收发生变化。诱导P-gp活性的药物预计会减少替诺福韦(韦立得、Vemlidy、TAF)的吸收,从而导致替替诺福韦(韦立得、Vemlidy)的血浆浓度降低,从而可能导致疗效丧失。替诺福韦(韦立得、Vemlidy、TAF)与其他抑制P-gp和BCRP的药物联合用药可能会增加替诺福韦酯的吸收和血浆浓度。
2、影响肾功能的药物
由于替诺福韦(韦立得、Vemlidy、TAF)主要通过肾小球滤过和活跃小管分泌的结合由肾脏排出,因此替诺福韦(韦立得、Vemlidy、TAF)与降低肾功能或竞争活跃小管分泌的药物合用可能会增加替诺福韦和其他肾脏消除药物的浓度,这可能会增加不良反应的风险。通过活跃的小管分泌消除的一些药物包括但不限于替诺福韦(韦立得、Vemlidy、TAF)、西多福韦、更昔洛韦、伐昔洛韦、缬更昔洛韦、氨基糖苷类药物(例如庆大霉素)和大剂量或多种非甾体抗炎药。
3、已建立的和其他潜在的重大相互作用
下表列出了已确定的或具有潜在临床意义的药物相互作用。所描述的药物相互作用是基于与替诺福韦(韦立得、Vemlidy、TAF)一起进行的研究,或者是预测的与替诺福韦(韦立得、Vemlidy、TAF)可能发生的药物相互作用。未提供与HIV抗逆转录病毒药物之间潜在药物相互作用相关的信息。该表包括潜在的重大相互作用,但并不包括全部。
表:确定的和其他潜在的显著药物相互作用a
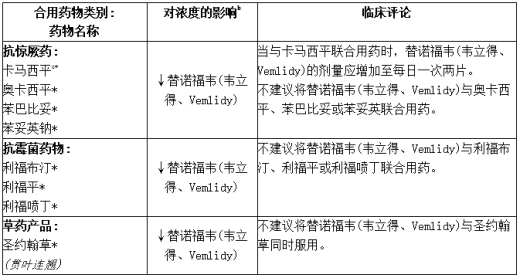
a表上并非全部
b↓=减少
c表明已经进行了药物相互作用的研究
* P-gp诱导剂
4、与替诺福韦(韦立得、Vemlidy、TAF)无明显临床相互作用的药物
根据与替诺福韦(韦立得、Vemlidy、TAF)进行的药物相互作用研究,未观察到与乙炔雌二醇、来地帕韦/索福布韦、咪达唑仑、诺估计、舍曲林、索福布韦、索福布韦/韦福帕布韦/韦帕帕韦的临床显著药物相互作用。
药物过量
如果发生药物过量,应监测患者是否出现中毒症状。替诺福韦(韦立得、Vemlidy、TAF)服用过量的治疗包括一般支持措施,包括监测生命体征和观察患者的临床状况。血液透析可有效清除替诺福韦,提取系数约为 54%。
成分
活性成分: tenofovir alafenamide
非活性成分:交联羧甲基纤维素钠、一水乳糖、硬脂酸镁和微晶纤维素。
片剂采用薄膜包衣,包衣材料包含:氧化铁黄、聚乙二醇、聚乙烯醇、滑石粉和二氧化钛。
性状
片剂
贮存方法
1、将替诺福韦(韦立得、Vemlidy、TAF)储存在30°C以下。
2、将替诺福韦(韦立得、Vemlidy、TAF)保存在其原始容器中。
3、保持容器紧密封闭。
4、替诺福韦(韦立得、Vemlidy、TAF)采用儿童安全包装。
5、请将替诺福韦(韦立得、Vemlidy、TAF)和所有药物放在儿童够不到的地方。


 医无忧服务热线:
医无忧服务热线:
