 400-028-6288
400-028-6288 在线客服
在线客服
 官方微信
官方微信
 400-028-6288
400-028-6288 在线客服
在线客服
 官方微信
官方微信

新闻动态

发表于 国际临床肿瘤学杂志
摘要
尿路上皮癌的治疗面临巨大挑战,尤其是在晚期阶段。传统上采用铂类化疗,免疫疗法(尤其是免疫检查点抑制剂)的出现彻底改变了尿路上皮癌的治疗。本综述探讨了尿路上皮癌治疗的演变,重点关注从免疫检查点抑制剂单药治疗到创新联合疗法的转变。继 KEYNOTE-045 试验之后,派姆单抗成为治疗经治疗的转移性尿路上皮癌的关键 ICI,其效果优于传统化疗。然而,未经治疗的转移性尿路上皮癌患者(尤其是 PD-L1 表达较低的患者)出现了局限性,IMvigor130 和 KEYNOTE-361 等试验证明了这一点。这些挑战促使人们探索联合疗法,包括免疫检查点抑制剂与铂类化疗、酪氨酸激酶抑制剂和抗体-药物偶联物。值得注意的是,CheckMate 901 试验表明,联合使用 nivolumab 和化疗可改善治疗效果。抗体-药物偶联物 enfortumab vedotin 和 pembrolizumab 的联合治疗取得了重大突破,为局部晚期或转移性尿路上皮癌的一线治疗树立了新标准。未来的方向包括进一步探索抗体-药物偶联物和免疫检查点抑制剂,如 TROPHY-U-01 和 TROPiCS-4 试验所示。该综述的结论是,局部晚期或转移性尿路上皮癌的治疗前景正在迅速发展,联合疗法为改善患者治疗效果提供了有希望的途径,标志着尿路上皮癌治疗的新时代。
介绍
尿路上皮癌 (UC) 起源于尿路上皮,可发生在肾盂、输尿管、膀胱和尿道等任何部位。在全球范围内,膀胱癌是第十大常见的癌症,UC 是其主要亚型。多年来,UC 的发病率一直在稳步上升,已成为重大的公共卫生问题。
几十年来,UC 的治疗,尤其是晚期和转移性 UC 的治疗,一直以铂类化疗为主。尽管这些方案提供了一些益处,但对于许多患者,尤其是那些化疗耐药或不适合治疗的患者,治疗效果仍然不理想。转移性 UC (mUC) 的 5 年生存率仅为 5-6%,这凸显了对更有效治疗策略的迫切需求。
近年来,人们对肿瘤与免疫系统之间相互作用的兴趣日益浓厚,并终促成了免疫疗法的发展,旨在利用人体免疫系统识别和对抗癌细胞。免疫检查点抑制剂 (ICI) 是一类免疫疗法,已成为肿瘤学界的希望之光。它们有可能彻底改变包括溃疡性结肠炎在内的多种癌症的治疗前景,已成为大量研究和临床试验的主题。
ICI 在 UC 治疗中的应用前景广阔,不仅可以改善生存结果,还可以提高生活质量。随着我们对这篇综述的深入研究,我们将探索 UC 免疫治疗的现状、挑战和未来前景,以深入了解这一快速发展的领域。
针对已接受治疗的 mUC 患者的 ICI 单药治疗的建立
免疫治疗在局部晚期或转移性尿路上皮癌 (la/mUC) 的二线治疗中的发展历程反映了癌症治疗的重大模式转变,标志着从传统化疗到靶向免疫治疗的转变。这一演变始于免疫疗法在这种背景下的首次引入,此后对其应用有了更成熟和更细致的理解 (表1 )。
表 1 ICI 单药治疗局部晚期或转移性尿路上皮癌一线或二线治疗的临床试验结果
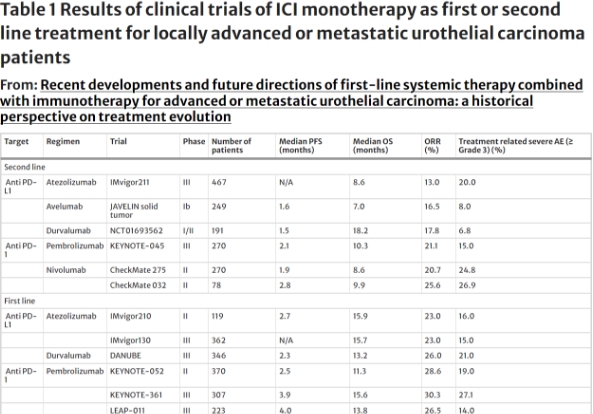
在 KEYNOTE-045 试验的结果公布后,派姆单抗在这一转变中的作用尤为突出。这项抗 PD-1 治疗性抗体的 III 期研究是一个里程碑,证明了派姆单抗在铂类化疗后出现进展的 la/mUC 患者中优于传统化疗方案紫杉醇、多西他赛或长春氟宁。该试验报告称,派姆单抗的中位总生存期 (mOS) 为 10.3 个月,而化疗为 7.4 个月,这使其成为新的标准治疗方法。长期随访结果进一步巩固了其地位,证实了其更高的生存率和中位反应持续时间。它还显示出对体能状态较差和老年患者一定的益处,而过去对这些患者来说化疗是困难的,并且它有助于拓宽治疗选择 。
相比之下,其他几种针对相同 PD-1/PD-L1 受体的药物并未显示出阳性的检测结果。尽管抗 PD-L1 治疗抗体 atezolizumab 初于 2016 年基于 IMvigor210 试验 获得美国食品药品监督管理局 (FDA) 批准,标志着免疫疗法应用的另一个早期成功案例,但随后的 III 期 IMvigor211 试验并未显示特定患者亚组的总生存期 (OS) 或反应率有显著改善。其他三种抗 PD-L1 治疗抗体 avelumab、durvalumab和抗 PD-1 治疗抗体 nivolumab在 III 期试验中也没有显示出显著改善。
免疫疗法作为 la/mUC 二线治疗的引入和确立代表了全科医学的重大进步。这强调了从传统化疗向利用人体免疫系统的更有针对性的方法的转变,尽管在优化其疗效和了解其长期影响方面仍存在持续的挑战和教育。
ICI 单药治疗对未接受治疗的 mUC 患者的局限性
几项关键临床试验的结果证实,将免疫疗法作为顺铂不适用患者 la/mUC 的主要治疗方法面临着重大挑战(表1)。FDA 于 2017 年批准了基于 II 期 IMvigor210和 KEYNOTE-052试验的阿替利珠单抗和帕博利珠单抗,这标志着一个充满希望的进展。在 IMvigor210 中,阿替利珠单抗的客观缓解率 (ORR) 为 23%,mOS 为 15.9 个月,中位无进展生存期 (mPFS) 为 2.7 个月。同时,KEYNOTE-052 报告帕博利珠单抗的 ORR 为 28.6%,mOS 为 11.3 个月。两项试验都表明,PD-L1 表达较高的患者的疗效更高。
在这种情况下,人们对安全性的担忧削弱了乐观情绪。在 KEYNOTE-052 中,67% 的患者经历了任何级别的不良事件 (AE),约 21% 的患者患有 ≥ 3 级 AE,包括结肠炎和肺炎。这些发现强调了谨慎选择和管理患者的必要性。
2018 年 5 月,欧洲药品管理局和 FDA 根据 III 期 IMvigor130和 KEYNOTE-361试验的早期数据发布了安全警报,情况进一步发展。这些试验表明,与接受铂类治疗的患者相比,接受 ICI 单药治疗的 PD-L1 表达较低的肿瘤患者的 OS 降低,尽管这两种药物仅推荐用于不适合接受任何铂类化疗的 la/mUC 患者。
尽管 ICI 在 la/mUC 中的初步结果令人鼓舞,但后续试验显示出其局限性,特别是在 PD-L1 表达低的患者中。
针对未经治疗的 mUC患者 的 ICI 联合疗法的开发
铂类诱导化疗后 ICI 维持治疗
诱导化疗对部分患者治疗la/mUC有效,但疗效不持久 。因此,有研究和报道,使用化疗、酪氨酸激酶抑制剂和聚 ADP 核糖聚合酶抑制剂等各种药物进行维持治疗可维持治疗效果。虽然回顾性分析报告了一定的疗效,但疗效的实际证据仍不清楚。III 期 JAVELIN Bladder 100 试验确立了阿维单抗作为铂类化疗后la/mUC 的维持治疗,代表了该疾病治疗的重大积极进展(表2)。试验结果显示,avelumab 的 mOS 为 23.8 个月,而对照组为 15.0 个月,这一结果确实值得注意,并凸显了免疫疗法在延长 la/mUC 患者生存期方面的潜力。
表 2 ICI 联合疗法作为局部晚期或转移性尿路上皮癌患者的一线治疗
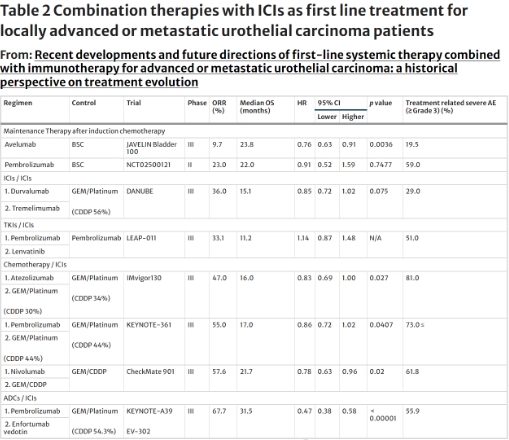
然而,除了这些积极成果之外,该试验的方法学方面也值得考虑,例如,在阿维单抗治疗之前允许进行 4-6 个疗程的诱导化疗。例如,在一项在类似环境中使用帕博利珠单抗的 II 期试验中,在从对照组交叉到治疗组后,观察到无进展生存期 (PFS) 有显著差异,但 OS 无差异。这一结果表明,早期维持治疗和延迟治疗之间可能没有差异。因此,在现实世界的实践中,4 个疗程后换用阿维单抗且病情稳定或更高,与 6 个疗程后使用帕博利珠单抗且病情恶化,这之间的差异无法明确,导致出现了更早使用阿维单抗的趋势。
另一个问题是,更换维持免疫疗法可能会导致病情迅速恶化,即所谓的超进展性疾病(HPD)。特别是在溃疡性结肠炎中,据报道,在几种癌症中,免疫疗法比化疗更容易发生HPD。据报道,HPD的危险因素包括高龄(> 65岁) 、女性、肝转移和高血清LDH、MDM2/MDM4扩增和EGFR异常。因此,临床医生在识别将从阿维单抗治疗中受益的患者的同时,也需要意识到弱势患者群体的存在。
这方面强调需要仔细解释生存益处,并通过平衡试验的积极结果与对其设计局限性的理解来考虑对临床实践中患者结果的潜在影响。
联合使用几种 ICI 治疗未接受治疗的 mUC 患者
III 期 DANUBE 试验探索了 durvalumab 和 tremelimumab(抗 CTLA-4 治疗性抗体)的 ICI/ICI 组合,但未达到其主要终点(表2)。该研究未能证明 durvalumab 单药治疗或联合治疗与化疗相比,mOS 有显著改善。对不适合顺铂治疗的患者进行的探索性分析表明,ICI/ICI 组合的 mOS 略有改善,但无统计学意义。
酪氨酸激酶抑制剂与 ICI 联合治疗未接受治疗的 UC 患者
有报道称,针对治疗选择有限的 la/mUC 患者,特别是那些不适合接受任何铂类化疗的患者,进行了 3 期临床试验 LEAP-011(表2)。该试验的突破性方法是首次将多激酶抑制剂仑伐替尼与免疫治疗药物派姆单抗结合起来。仑伐替尼靶向 VEGF 受体、成纤维细胞生长因子受体 (FGFR) 受体和其他受体和致癌基因。这种组合背后的原理是基于这样的理解:VEGF 上调在实体肿瘤的血管生成中起着至关重要的作用,而 FGFR 基因的改变在UC 患者中很常见。
在试验中,487 名患者被随机分配接受仑伐替尼加帕博利珠单抗或安慰剂加帕博利珠单抗的联合治疗。然而,结果并未显示联合治疗优于单独使用帕博利珠单抗。联合治疗组的 mPFS 为 4.5 个月,而帕博利珠单抗组为 4.0 个月,mOS 分别为 11.8 个月和 12.9 个月。此外,联合治疗组的 3-5 级不良事件发生率更高。
LEAP-011 研究结果表明,与单独使用派姆单抗相比,乐伐替尼和派姆单抗联合治疗晚期 UC 患者的疗效并未改善,因此该试验因此提前终止。这一结果凸显了为该患者群体开发有效且耐受性好的治疗方案的持续挑战,并强调需要继续研究新的治疗组合。
化疗和 ICI 联合治疗未接受治疗的 UC 患者
IMvigor130 和 KEYNOTE-361 III 期试验评估了免疫疗法与化疗联合治疗 la/mUC 的效果,结果表明,与单纯化疗相比,免疫疗法联合治疗在改善患者预后方面的疗效有限(表2)。
在 IMvigor130 试验中,1213 名 la/mUC 患者随机接受阿替利珠单抗联合铂类化疗(吉西他滨加顺铂或卡铂)、单独接受阿替利珠单抗或单独接受铂类化疗。尽管将阿替利珠单抗加入化疗可略微改善 mPFS(8.2 个月 vs. 6.3 个月,p =0.014),但未达到 OS 这一关键的共同主要终点。阿替利珠单抗联合化疗的效果并不明显优于单独化疗(16.0 个月 vs. 13.4 个月,p =0.054)。
同样,KEYNOTE-361 试验招募了 1010 名 la/mUC 患者,接受帕博利珠单抗单药治疗、铂类化疗或两者联合治疗。经过中位随访 31.7 个月后,与单纯化疗相比,帕博利珠单抗加化疗并未显著改善 PFS 或 OS。帕博利珠单抗组和化疗组的 mOS 相似(15.6 个月 vs. 14.3 个月),即使在 PD-L1 表达高(CPS ≥ 10%)的患者中也是如此。
这些试验凸显了在 la/mUC 中通过添加免疫疗法来增强标准化疗效果的挑战。尽管抱有希望,但联合疗法并未显著改善 OS,这导致人们重新评估这些免疫疗法在一线治疗中的作用。因此,目前的指南变得更加严格,根据 PD-L1 表达和铂类化疗的适用性将这些免疫疗法的使用限制在特定患者群体中。
但幸好,多国开放标签的 3 期 CheckMate 901 试验终于成为不可切除或 mUC 治疗的一个重要里程碑。该研究首次证明了化疗与免疫治疗联合治疗在改善 OS 方面的疗效,而单纯化疗则不然。
该试验纳入了 608 名患者,每组 304 名。在中位随访期 33.6 个月中,结果非常显著。接受 nivolumab 联合治疗的组的 OS 明显更长,中位生存期为 21.7 个月,而仅接受化疗的组为 18.9 个月。死亡风险比为 0.78,表明使用 nivolumab 联合治疗后死亡风险降低了 22%。PFS 也有利于 nivolumab 组,风险比为 0.72,反映出疾病进展或死亡风险降低了 28%。与仅接受化疗的组(7.6 个月)相比,nivolumab 联合治疗组的 mPFS 略长(7.9 个月)。
此外,nivolumab 联合治疗组的整体 ORR 更高,为 57.6%,其中 21.7% 的患者达到完全缓解,而仅化疗组为 43.1%(完全缓解 11.8%)。nivolumab 联合治疗的完全缓解持续时间中位数(37.1 个月)也显著长于仅化疗组(13.2 个月)。然而,nivolumab 联合治疗组(61.8%)发生 3 级或以上不良反应的几率高于仅化疗组(51.7%)。
目前尚不清楚为何 CheckMate 901 研究是一项获得阳性结果的研究,而另外两项研究则不然。原因之一可能是 CheckMate 901 中使用的铂类药物只有顺铂,并且只选择了一般状况较好且肾功能不差(GFR < 60 ml/min)且 ECOG PS 较差(≧2)的患者。在二线治疗中接受 ICI 治疗的患者中,根据一线使用的铂类药物类型,顺铂的预后更好,但在调整体能状态和其他参数后无差异。换句话说,能够接受顺铂治疗的患者更可能一般状况良好,这可能使免疫治疗的治疗效果更高,正如之前在二线和更多情况下所报告的那样。NILE 试验 (NCT03682068) 是一项关键的 III 期研究,旨在检验在 la/mUC 的标准化疗中添加 durvalumab(联合或不联合 tremelimumab)的疗效。人们热切期待其主要终点 OS,因为它可能会重新定义这种疾病的早期治疗方法。
ADC 与 ICI 联合治疗未经治疗的 mUC 患者
抗体药物偶联物 (ADC) 与 ICI的结合在 la/mUC 治疗方面取得了突破性进展(表2)。ADC 是一种新型治疗药物,由与细胞毒性药物相连的抗体组成,可将化疗药物靶向递送至肿瘤细胞,同时大限度地减少全身暴露和潜在副作用。该试验重点关注 enfortumab vedotin (EV) 的疗效,这是一种靶向 nectin-4 的 ADC,nectin-4 是一种在 UC 细胞中高度表达的蛋白质。EV 与强效细胞毒性药物偶联,该药物已获批用于对 ICI 有耐药性的 la/mUC 患者。
IB/II 期 EV-103/KEYNOTE-869 研究为 FDA 加速批准该组合用于不适合含顺铂化疗的 la/mUC 患者提供了依据。在这项多队列研究中,确认的 ORR 高达 73.3%,剂量递增和剂量扩展队列中的完全缓解率为 15.6%。此外,中位缓解持续时间为 25.6 个月,凸显了这种治疗方法的持久性。
III 期 EV-302/KEYNOTE-A39 试验比较了 EV 联合帕博利珠单抗与标准铂类化疗(吉西他滨加顺铂或卡铂)的疗效。该试验评估了这种联合疗法的有效性和安全性,无论患者是否适合使用顺铂以及 PD-L1 表达状态如何。该试验的主要终点是 PFS 和 OS。与化疗相比,这种联合治疗显著改善了 PFS 和 OS。mPFS 延长至 12.5 个月(化疗为 6.3 个月),mOS 达到 31.5 个月(化疗为 16.1 个月)。联合治疗还实现了更高的确认 ORR,为 67.7%。虽然观察到了 3 级治疗相关 AE,但这些不良反应通常可控,未报告新的安全信号。
此次试验不仅通过成功结合 ADC 与 ICI 标志着 la/mUC 治疗的一个重要里程碑,而且还为 la/mUC 的一线治疗建立了新的护理标准,在可控的安全性下显著改善了患者的治疗效果。
未来发展方向
正在进行的 la/mUC 领域临床试验的新数据表明,ADC 和 ICI 联合治疗前景光明。这些创新疗法有望重新定义 la/mUC 的治疗前景,该领域对更有效、更耐受的疗法的需求仍然很大(表3)。
表 3 针对局部晚期或转移性尿路上皮癌患者的 ADC 与 ICI 联合临床试验正在进行中

TROPHY-U-01 研究针对 la/mUC 中的 sacituzumab govitecan (SG),其不同队列针对不同的患者群体,已取得令人鼓舞的结果。队列 1 的结果促使 FDA 加速批准 SG,这表明 ADC 对标准铂类化疗和 ICI 治疗后进展的患者有效。队列 2 的积极结果侧重于不适合铂类治疗的患者,进一步凸显了 ADC 在更广泛患者群体中的潜力。此外,队列 3 中 SG 与 pembrolizumab 的联合治疗尤其值得注意,其 ORR 为 41%,mOS 为 12.7 个月。这些结果表明,ADC 与 ICI 的联合治疗可以增强治疗效果,超过任何一种方法单独使用时所能达到的效果。正在进行的 III 期 TROPiCS-4 试验 (NCT04527991) 对初始治疗失败后的 SG 与化疗进行了比较,预计将为 ADC 在后期治疗方法中的效用提供更多见解。
另一个关键领域 HER2 靶向治疗的平行进展也在重塑 la/mUC 的治疗策略。在约 10% 的 la/mUC 患者中发现了 HER2 基因扩增。来自 disitamab vedotin 的研究和即将进行的试验(例如 RC48G001 和 disitamab vedotin 联合特瑞普利单抗与化疗对比的 III 期试验)的结果为针对 HER2 表达的 la/mUC采取更有针对性的治疗方法奠定了基础。
与这些试验同时进行的研究重点是寻找可预测 ICI 疗效的生物标志物。虽然 PD-L1 表达是研究,但新兴的生物标志物(如肿瘤突变负荷、DNA 损伤修复改变、CD8 T 细胞的肿瘤浸润、微卫星不稳定性高状态 、消化道内的微生物组、局部肿瘤组织和血液)正在引起人们的关注。“尿路上皮癌免疫图”的概念正在开发中,以预测对免疫疗法的疗效,但其临床应用仍处于起步阶段。
正在进行的研究 MORPHEUS-UC (NCT03869190) 和 JAVELIN Bladder Medley (NCT05327530) 正在研究各种新型组合,包括 ICI 与 ADC、PARP 抑制剂、抗 CD47、抗 TIGIT 和细胞因子受体激动剂。这些试验旨在解决对单药免疫疗法的耐药性问题,并探索不同类别疗法之间的协同作用。
结论
la/mUC 治疗领域正处于重大变革的前沿,许多试验正在探索 ICI 与传统和新型疗法的结合。这些研究旨在改善患者的治疗效果,并扩大有效治疗的范围,标志着 UC 管理领域一个激动人心的时代到来。


 医无忧服务热线:
医无忧服务热线:
